 Enzymatic Debridement with Bromelain
Enzymatic Debridement with Bromelain
Dra. Pamela A. Quintanilla Calatayud
Médico
Especialista en Cirugía General
Estudiante de la carrera de post grado de Cirugía Plástica y Reparadora de la Universidad Del Salvador
Rotación Quemados
Hospital Alemán
Agosto- Diciembre 2022
Profesor: Dr. Alberto Bolgiani
Pamelaquintanillac@gmail.com
Resumen
El desbridamiento enzimático de las quemaduras que alcanzan y afectan la dermis profunda o el tejido subcutáneo es una alternativa al desbridamiento quirúrgico habitual. Mediante un fármaco de origen biológico que contiene un concentrado liofilizado de enzimas proteolíticas (EP) enriquecido con bromelína, esto ha generado un nuevo escenario terapéutico en el tratamiento de las quemaduras térmicas de espesor parcial profundo y completo. Los resultados muestran que el preparado con enzimas proteolíticas con bromelína presenta ventajas respecto al desbridamiento quirúrgico en pacientes con quemaduras de segundo grado intermedio y profundo, siempre que se realice de forma protocolizada y bajo los criterios de administración y posología indicados.
Material y métodos: Revisión Bibliográfica.
Resultados y conclusiones: Se demostró que el desbridamiento enzimático proteolítico derivado del ananá, podría tratarse de una evolución en el tratamiento del quemado, pudiendo sustituir los tratamientos actuales, mediante la especificidad de su acción, actuando sobre el tejido necrótico sin afectar el tejido viable. Rapidez de acción y prácticamente una sola dosis de aplicación.
Palabras clave: Bromelína, desbridamiento quirúrgico, desbridamiento enzimático, quemaduras.
Summary
Enzymatic debridement of burns that reach and affect the deep dermis or subcutaneous tissue is an alternative to routine surgical debridement. Through a drug of biological origin that contains a lyophilized concentrate of proteolytic enzymes (EP) enriched with bromelain, this has generated a new therapeutic scenario in the treatment of deep and complete partial thickness thermal burns. The results show that the preparation with proteolytic enzymes with bromelain presents advantages with respect to surgical debridement in patients with intermediate and deep second-degree burns, provided that it is carried out in a protocolized manner and under the indicated administration and dosage criteria.
Material and methods: Bibliographic review.
Results and conclusions: it was demonstrated that the proteolytic enzymatic debridement derived from pineapple could be an evolution in the treatment of burns, being able to replace current treatments, through the specificity of its action, acting on necrotic tissue without affecting viable tissue. Speed of action and practically a single dose of application.
Key words: Bromelain, surgical debridement, enzymatic debridement, burns.
Introducción
El tratamiento precoz mediante desbridamiento constituye el tratamiento estándar de atención para las quemaduras que se extienden hacia y más allá de la dermis profunda. Ya que el desbridamiento temprano reduce las tasas de infección y complicaciones, acorta las estadías en el hospital y mejora la cicatrizacion de heridas por quemaduras en comparación con el desbridamiento tardío de estas quemaduras. Sin embargo, el desbridamiento quirúrgico desafía a los pacientes con considerable dolor, sangrado, pérdida de calor, y una mala diferenciación entre el tejido viable y muerto, lo que resulta en una escisión innecesaria de tejido sano para alcanzar un plano subsidiario de recibir autoinjertos (1).
El concentrado de enzimas proteolíticas enriquecidas con bromelína, es un agente desbridante enzimático de aplicación tópica. Está indicado para la retirada de las escaras por quemadura de origen térmico en quemaduras de espesor parcial y/o completo hasta las 48 horas después. Su eficacia clínica y seguridad han sido demostradas en diversos estudios disminuyendo el porcentaje de pacientes que requieren autoinjertos y la superficie injertada, con bajas tasas de cicatrización hipertrófica (2).
Materiales y Métodos
Se realizó revisión literal ingresando a las diferentes plataformas digitales (revista, sociedades, pubmed). En las cuales se menciona la experiencia, eficacia y seguridad del uso de enzimas proteolíticas enriquecidas con bromelína para tratamiento terapéutico, en el desbridamiento de quemaduras térmicas.
Epidemiologia
Se estima que durante un año calendario el 1% de la población sufre una quemadura que requiere manejo por un agente de salud entrenado. Sin embargo, la edad de los lesionados, así como su extensión y el tipo de quemadura varían de acuerdo con las características de desarrollo en materia de salud, las condiciones laborales y el clima. En efecto, mientras en los lugares con mayor desarrollo industrial las quemaduras son más frecuentes por llama o accidentes de trabajo; en los sitios con mayor pobreza se producen por líquido caliente como resultado de accidentes domésticos (3).
CLASIFICACION
Las quemaduras se clasifican en:
Grado I. Corresponden a las quemaduras producidas por exposición solar, en las cuales se compromete la epidermis únicamente. Se produce descamación en los siguientes 7 a 10 días, y no queda cicatriz ni cambios de coloración (3).
Grado II. La lesión alcanza grados variables de la dermis. Estas quemaduras cuando son superficiales se les denomina Tipo A y cicatrizan en un plazo inferior a 14 días sin dejar secuelas importantes. Sin embargo cuando destruyen una parte importante de la dermis, la cicatrización se produce después de los 18 días y la cicatriz es de mala calidad, con aparición de queloide, hiper o hipopigmentación y retracciones. Esta quemadura también se llama tipo AB (3).
Grado III. La lesión que destruye toda la dermis, y que por lo tanto no deja restos dérmicos o epidérmicos que permitan la epitelización. La cicatrización se produce por segunda intención, es decir por aproximación de los bordes de la superficie cruenta, y la epitelización solo alcanza uno o dos centímetros desde el borde de piel sana. Para obtener una epitelización completa se requiere desbridar hasta obtener tejido de granulación e injertar. Estas quemaduras se denominan también tipo B (3).
Grado IV. Implica destrucción de músculo o estructuras óseas. Generalmente son el resultado de la energía por electricidad (3).
FISIOPATOLOGIA
En paciente con quemaduras severas representa un modelo de trauma grave que se caracteriza por una gran variedad de eventos fisiopatológicos, la mayoría muy bien estudiados.
- El Edema. Se debe a un secuestro de líquido en el espacio intersticial, el cual es muy rápido en los primeros minutos y continúa durante las primeras 24 horas. Mediante cambios en la permeabilidad capilar, a los cuales se suma el incremento en la presión hidrostática por el suministro de líquidos endovenosos y la disminución de la presión oncótica del plasma (3).
- Los Trastornos Hemodinámicos. Después de la injuria térmica tanto el índice cardíaco como la resistencia vascular sistémica se comportan de acuerdo a la hipovolemia existente y al resultado de la resucitación con líquidos endovenosos. El fenómeno inicial de los pacientes quemados parece ser una hipoperfusión tisular muy severa que se inicia en forma precoz, desde los cinco minutos después del trauma. Esta hipoperfusión se debe a una hipovolemia por el secuestro de líquidos ya descrito, y a una vasodilatación secundaria a los mediadores que se originan en el lugar de la lesión térmica (3).
- La Profundización. Casi siempre existen diferentes grados de profundidad en las áreas lesionadas, los cuales varían de acuerdo a la distancia existente desde el punto de máxima lesión. Estas zonas, conocidas como las zonas de Jackson, son las siguientes:
Zona de necrosis: En el lugar de la quemadura de espesor total, la lesión anatomopatológica es necrosis por coagulación. El examen microscópico en este lugar muestra ausencia de restos dérmicos (3).
Zona de estasis: En la cual se observa obliteración de la microvasculatura. Esta zona va a evolucionar hacia la necrosis en las siguientes horas (3).
Zona de hiperemia: Se trata de quemaduras de espesor parcial, las cuales pueden evolucionar hacia la mejoría o hacia la necrosis de acuerdo al tipo de terapia instaurada (3).
Concentrado de enzimas proteolíticas enriquecidas con bromelína
La Agencia Europea del Medicamento aprobó en 2012, por procedimiento centralizado y medicamento huérfano (Nexobrid), indicado para la extracción de escaras en adultos con quemaduras térmicas de un espesor parcial profundo y completo. Posteriormente, fue autorizado y comercializado por la Agencia Española del Medicamento en 2014. La Food and Drug Administration aún no lo ha autorizado (4).
Las enzimas proteolíticas presentes en Ananás comosus, son del tipo cisteína peptidasa y las más estudiadas son: bromelína del tallo, bromelína del fruto, Ananaina y Comosaina, todas ellas están presentes en un extracto acuoso obtenido del tallo y/o fruto de la piña conocido como bromelína.
Estas cisteínas peptidasas han demostrado tener propiedades terapéuticas en la actividad antiedematosa, antiinflamatorias al modular las moléculas de la superficie celular de los leucocitos como CD 14, CD 44, CD 16, CD 21, CD 128 a y b que están involucradas en la búsqueda de leucocitos, adhesión celular, inducción de mediadores proinflamatorios y efecto inmunomodulador sobre las células T mediante la inhibición de la transducción de señales de células T, produciendo efecto sobre Th1, Th2 y citoquinas inmunosupresoras, también reduce el reclutamiento de neutrófilos mediado por P-selectina (5), antitrombóticas, fibrinolitica, antitumoral, antimetastásica, inmunomodulador, promotora de la absorción de antibióticos, debridante de heridas y cicatrizante (6).
Se trata de una mezcla parcialmente purificada de EP enriquecidas con bromelína, extraída del tallo de la planta de piña (Ananás comosus), que contiene principalmente proteasas, en una solución de ácido acético y sulfato de amonio, está indicado en la extracción de escaras en adultos con quemaduras térmicas de un espesor parcial profundo y completo, y actúa sobre el tejido necrosado, respetando el tejido sano (4)..
Procedimiento
La mezcla de enzimas proteolíticas, debe aplicarse a la lesión húmeda, limpia y sin queratina (después de la extracción de las ampollas). Deben retirarse los medicamentos de uso tópico y limpiar la herida antes de su aplicación; además, se debe usar antes de 15 minutos una vez preparada la mezcla y no debe aplicarse a más de un 15% de la superficie corporal total (SCT). No se ha establecido todavía la seguridad y la eficacia del producto en niños y adolescentes menores de 18 años (4).
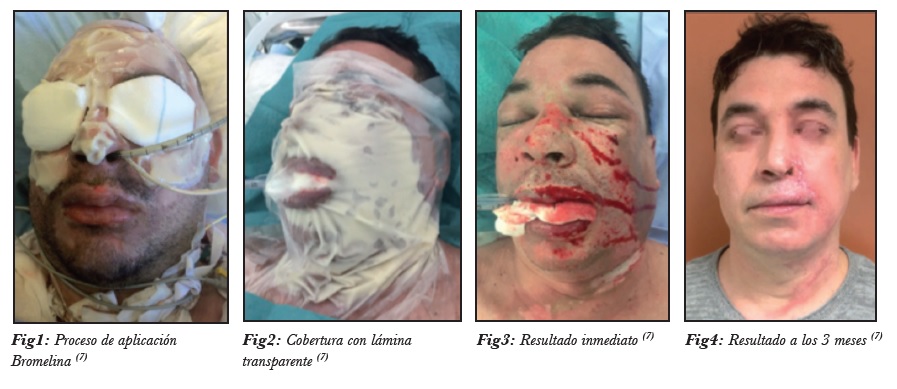
Se dejá una cura húmeda con Clorhexidina jabonosa al 0.5% durante al menos 2 horas, para aplicar el producto el paciente debe encontrarse bajo anestesia regional o sedoanalgesia. La cantidad a aplicar es de 2 gr por cada 1% de SCT (2). Extendemos esta mezcla sobre la zona a tratar, en una capa de 1.5 a 3 mm de espesor (fig 1), que cubrimos después con una lámina transparente estéril durante las 4 horas que dura su aplicación (fig 2). Una vez superado el periodo de desbridamiento, retiramos cuidadosamente todos los restos del desbridante mediante arrastre con gasas embebidas en suero fisiológico. Tras retirar completamente el producto, se evalúa la eficacia del desbridamiento (fig 3), y en cada caso si es precisa una nueva aplicación, que se realizaría transcurridas 24 horas (7). Aquellos casos en los que la profundidad de la quemadura obligaba a injertar, se deja una cura con apósito hidrocoloide hasta la cobertura definitiva mediante autoinjerto de piel, en aquellos casos que podrían alcanzar la epitelización espontánea mediante cura dirigida se cubre mediante apósito sintético (2).
Los medicamentos antibacterianos de uso tópico (sulfadiazina argéntica o povidona yodada) pueden reducir la eficacia del concentrado de EP. La bromelína puede potenciar los efectos del fluorouracilo y la vincristina, así como el efecto hipotensor de los inhibidores de la enzima convertidora de angiotensina y la somnolencia causada por algunos medicamentos depresores del sistema nervioso central (4).
Conclusión
Cabe destacar que la utilización de EP enriquecidas con bromelína para el desbridamiento enzimático de quemaduras de un espesor profundo y completo es una buena alternativa al tratamiento quirúrgico convencional. La elevada selectividad por el tejido necrosado de la quemadura evita la lesión de la dermis viable adyacente o subyacente a la misma, y reviste una particular importancia en las quemaduras profundas del dorso de la mano y los dedos, con escaso tejido subdérmico, donde el desbridamiento quirúrgico es técnicamente complejo y puede lesionar estructuras profundas, como los paquetes neurovasculares o los tendones extensores. Por otro lado, la presencia de remanentes dérmicos en el lecho desbridado permite, en muchos casos, su reepitelización sin necesidad de injertarlo, evitando así la realización de nuevas heridas y las consiguientes cicatrices en zonas dadoras. Hasta el momento, el uso de concentrado de EP se limita a las quemaduras térmicas (por llama, escaldadura o contacto). Su uso no está aconsejado en las quemaduras eléctricas, en las que el mecanismo lesional es complejo y las estructuras profundas (como el hueso) resultan afectadas en mayor medida; tampoco en las quemaduras de etiología química o impregnada con sustancias radiactivas y otras sustancias nocivas. Además, se ha observado que el desbridamiento enzimático se ve limitado cuando se aplica en quemaduras cubiertas previamente con medicamentos antibacterianos de uso tópico, como la povidona yodada o la pomada de sulfadiazina argéntica, que forma una pseudoescara característica sobre la quemadura, impidiendo la adecuada penetración del producto (4).
En resumen, las potenciales ventajas del uso de concentrado de EP son las siguientes:
- Menor necesidad de escisión quirúrgica, con la consiguiente disminución de las complicaciones asociadas (4).
- Mejora de la logística de las unidades de quemados, al poder realizarse el procedimiento en la habitación del paciente, sin precisar un quirófano, con personal de enfermería entrenado y la colaboración del equipo de anestesiología (4).
- Posibilidad de realizar un desbridamiento precoz también en las quemaduras en que coexisten diferentes grados de profundidad, lo que disminuiría la liberación de mediadores inflamatorios y el riesgo de infección de la escara (4).
- Posibilidad de realizar un desbridamiento selectivo y menos traumático, evitando la lesión del tejido sano y facilitando la persistencia de remanentes dérmicos viables en el lecho desbridado, lo que disminuye la necesidad de autoinjertos (4).
Bibliografía
-
Laura Bolton, Desbridamiento de quemaduras ¿estamos optimizando los resultados?, rincón de la evidencia, Diciembre 2019. https://www.hmpgloballearningnetwork.com/site/wounds/evidence-corner/burn-debridement-are-we-optimizing-outcomes.
-
JR Martínez-Méndez, Á Sanz-Granda, Á González-Miranda, Á Ojeda-Regidor, C Casado-Pérez. Estudio económico del tratamiento de las quemaduras térmicas mediante desbridamiento enzimático; papel determinante de la estancia hospitalaria Cir. plást. iberolatinoam. vol.44 no.2 Madrid abr./jun. 2018 Epub 08-Feb-2021.
-
Ferrada R. Cirugía de Emergencias. Distribuna Editorial. Sección III. Trauma. 21 Guía de Quemaduras. Manejo inicial.
-
J Serracanta, A. Monte Soldado, Desbridamiento selectivo en quemaduras térmicas mediante enzimas proteolíticas enriquecidas con bromelína, Article in Farmaceutico Hospitales · Mayo 2018 https://www.researchgate.net/publication.
-
A Muhammad, T Ahmad. Therapeutic uses of pineapple-extracted bromelain in surgical care — A review Zehra, Journal of the Pakistan Medical Association, Enero 2017, volumen 67, número 1
-
RR Caceres. Debridante enzimático proteolítico derivado del Ananá. Revista argentina de quemaduras. Volumen 26, Nº2 agosto 2016.
-
J-M Sampietro-De-Luis, P López-Cabrera, Á-J Bernal-Martínez, V Yuste-Benavente y A Agulló-Domingo. Experiencia con Nexobrid® para el desbridamiento enzimático de quemaduras faciales seguido de tratamiento conservador con Medihoney. Cir.plàst.iberolatinoam.-Vol.42-Nº3 Julio-Agosto-Septiembre 2016/ pág. 217-225

