TGF-β/SmadPathway and how to attenuate tissue fibrosis
Dr. León Martin J.
Trabajo Final
Rotación de Quemados
Carrera de Especialista en Cirugía Plástica, Reconstructiva y Reparadora
Universidad del Salvador
Dr. Alberto Bolgiani
Datos de contacto del autor: martinjleon87@gmail.com – +54 9 381 5762382
RESUMEN
Las cicatrices aberrantes de la piel, incluidos los queloides y las cicatrices hipertróficas, se caracterizan por la formación y deposición excesivas de colágeno, es el resultado final del proceso patológico de cicatrización de heridas. La vía de señalización TGF-β/Smad en los fibroblastos y miofibroblastos está involucrada en el proceso de cicatrización de la fibrosis cutánea, la misma es una respuesta de cicatrización de heridas a una lesión celular aguda o crónica que se caracteriza por la acumulación de matriz extracelular (ECM). La evidencia excesiva demostró que la fibrogénesis está asociada con el sistema renina-angiotensina, la inflamación y el estrés oxidativo, la vía de señalización del factor de crecimiento transformador β (TGF-β)/Smad, la vía de señalización Wnt/β-catenina y el metabolismo de los lípidos. Entre ellos, la señalización TGF-β/Smad juega un papel importante en la fibrosis. El TGF-β se encuentra en la matriz en un estado latente y debe activarse antes de que pueda unirse a sus receptores. En los últimos años, se ha prestado más atención a la vía de señalización TGF-β/Smad como objetivo eficaz de la terapia antifibrótica, que además, es la vía más canónica a través de la cual se regula la formación de colágeno en los fibroblastos y miofibroblastos. Hay dos categorías de estrategias terapéuticas que tienen como objetivo dirigirse a la vía de señalización TGF-β/Smad en fibroblastos y miofibroblastos para interferir con sus funciones celulares y reducir la proliferación celular. La primera estrategia terapéutica incluye medicamentos, y la segunda estrategia se compone de terapia genética y celular. Por lo tanto, el objetivo de esta revisión es evaluar críticamente estas dos estrategias terapéuticas principales que se dirigen a la vía TGF-β/Smad para atenuar la formación anormal de cicatrices en la piel.
Palabras Clave: Cicatriz hipertrófica, queloide, fibroblastos, TGF-β/Smad, estrategias terapéuticas.
ABSTRACT
Aberrant skin scars, including keloids and hypertrophic scars, are characterized by excessive collagen formation and deposition, is the end result of the pathological process of wound healing. The TGF-β/Smad signaling pathway in fibroblasts and myofibroblasts is involved in the healing process of skin fibrosis, which is a wound-healing response to acute or chronic cell injury characterized by matrix accumulation extracellular (ECM). Excessive evidence demonstrated that fibrogenesis is associated with the renin-angiotensin system, inflammation and oxidative stress, the transforming growth factor-β (TGF-β)/Smad signaling pathway, the Wnt/β-catenin signaling pathway and lipid metabolism. Among them, TGF-β/Smad signaling plays an important role in fibrosis. TGF-β is in the matrix in a latent state and must be activated before it can bind to its receptors. In recent years, more attention has been paid to the TGF-β/Smad signaling pathway as an effective target of antifibrotic therapy, which is also the most canonical pathway through which collagen formation in fibroblasts is regulated. and myofibroblasts. There are two categories of therapeutic strategies that aim to target the TGF-β/Smad signaling pathway in fibroblasts and myofibroblasts to interfere with their cellular functions and reduce cell proliferation. The first therapeutic strategy includes drugs, and the second strategy consists of gene and cell therapy. Therefore, the aim of this review is to critically evaluate these two main therapeutic strategies that target the TGF-β/Smad pathway to attenuate abnormal skin scar formation.
Keywords: Hypertrophic Scar; Keloid; Fibroblast; TGF-β/Smad; Therapeutic strategies.
MATERIALES Y MÉTODOS
Se realizó una búsqueda bibliográfica en Pubmed utilizando palabras clave Hypertrophic Scar; Keloid; Fibroblast; TGF-β/Smad; Therapeutic strategies, donde se encontraron un total de 25 artículos, de los cuales 10 de ellos tienen relación con fibrosis tisular y vías de señalización TGF-β/Smad, el resto se excluyó por estar relacionado con fibrosis hepática, renal, carcinogénesis y temas no afines a la fibrosis tisular.
INTRODUCCIÓN
La piel es un órgano del sistema tegumentario que actúa como una barrera externa suave para cubrir los músculos, huesos, nervios y órganos internos subyacentes y es la primera línea de defensa contra factores externos. Hay muchos estímulos externos destructivos que pueden conducir a lesiones cutáneas en la piel, como trauma, quemaduras y cirugía. La formación de cicatrices se produce como resultado de lesiones en la piel y puede conducir a una alteración de la estética o a una función reducida de la piel y trastornos psicológicos (1,2). Por lo tanto, el estudio de los mecanismos moleculares de formación de cicatrices es importante para desarrollar una mejor comprensión del proceso con el fin de reducir la formación de cicatrices, prevenir el deterioro de la función de la piel y mejorar la apariencia. La formación de cicatrices es un componente del proceso de cicatrización de heridas, que es un proceso fisiológico normal, complejo y estrictamente regulado que implica la migración celular, la inflamación, la inervación y la angiogénesis. Sin embargo, un proceso patológico de cicatrización de heridas puede conducir a la formación de cicatrices desorganizadas, que se caracteriza por una fibrosis excesiva.
Las cicatrices anormales en la piel incluyen la formación de dos tipos diferentes de cicatrices, queloides e hipertróficas, que tienen diferentes características clínicas. Una cicatriz hipertrófica es una cicatriz ancha, espesa y a menudo elevada que se desarrolla en el sitio de la lesión cutánea que puede picar y que normalmente no se extiende más allá del límite de la herida original. Una de las principales causas de la formación de cicatrices hipertróficas es la tensión mecánica en la herida (3), pero suelen sufrir una regresión espontánea en uno o dos años. Las cicatrices queloides son lesiones elásticas duras o nódulos fibrosos brillantes asociados con el prurito y el dolor. Las cicatrices queloides se consideran tumores benignos, pero a menudo se identifican erróneamente como tumores malignos debido a su apariencia clínica, se extienden más allá del límite del sitio original de la lesión cutánea e invaden los tejidos adyacentes. Las personas con cualquier nivel de trauma cutáneo, incluyendo cirugía, piercings, acné, tatuajes, picaduras de insectos, quemaduras, laceraciones, abrasiones, vacunas y cualquier otro proceso que resulte en inflamación cutánea, están predispuestas al desarrollo de cicatrices hipertróficas y queloides (4,5). Ambos tipos de cicatrices están asociados con una fibrosis excesiva causada por la sobreproducción y la deposición en exceso de matriz extracelular (ECM), compuesta principalmente por colágeno, en cicatrices hipertróficas hay niveles elevados de colágeno paralelo tipo III y en cicatrices queloides un exceso de colágeno desorganizado de tipo I y III (5).
La desregulación de la señalización TGF-β/Smad es un factor importante en el marco de las cicatrices y la fibrosis, lo que conduce a la síntesis y deposición patológica de colágeno, una mayor proporción de colágeno I/III y la formación de haces de fibra de colágeno anormalmente reticulados (6,7,8). El TGF-β desempeña un papel fundamental en la producción del fenotipo de miofibroblastos que es responsable de la deposición masiva de colágeno y la contracción de las heridas (9).
El TGF-β1 se considera un mediador crucial en la fibrosis tisular y causa cicatrices tisulares en gran medida al activar a su señalización decapentapléjica (Smad). TGF-β1 activa directamente la señalización de Smad, lo que desencadena la sobreexpresión del gen profibrótico. Estudios excesivos han demostrado que la desregulación de la vía TGF-β1/Smad era un mecanismo patógeno importante en la fibrosis tisular. Smad2 y Smad3 son los dos principales reguladores que promueven la fibrosis tisular mediada por TGF-β1, mientras que Smad7 sirve como un regulador de retroalimentación negativa de la vía TGF-β1/Smad, lo que protege contra la fibrosis.
TGF-β es un mediador multifuncional que regula la proliferación, la diferenciación, la apoptosis, la adhesión y la migración en varias células, como los macrófagos, las células T y B activadas, las células hematopoyéticas inmaduras, los neutrófilos y las células dendríticas. Hay tres isoformas de TGF-β, incluyendo el factor de crecimiento transformador β1 (TGF-β1), el factor de crecimiento transformador β2 (TGF-β2) y el factor de crecimiento transformador β3 (TGF-β3). TGF-β1 se expresa en células de tejido endotelial, hematopoyético y conectivo, y TGF-β2 se expresa en células epiteliales y neuronales, mientras que TGF-β3 se expresa principalmente en células mesenquimales.
El bloqueo de TGF-β neutralizando los anticuerpos TGF-β, la decorina y los oligonucleótidos previene o mejora la fibrosis. La decorina es un proteoglicano pequeño, puede ser celular o de ECM se caracteriza por poseer una región rica en leucinas con una cadena de glicosaminoglicanos que bien puede ser del tipo condroitín sulfato o bien del tipo dermatán sulfato.
La expresión génica de TGF-beta(1), smad2 y smad3 podría detectarse en la piel fetal y después del nacimiento. En la piel del feto gestacional temprano, las expresiones genéticas de TGF-beta(1) y smad2 son débiles. Junto con el avance de la edad gestacional, la expresión génica en la piel se hace cada vez más fuerte. En la del feto gestacional tardío y en la piel después del nacimiento, el contenido de transcripción de estos dos genes aumenta significativamente en comparación con el feto gestacional temprano. Por el contrario, la expresión génica de smad3 fue aparentemente más alta en la piel fetal más joven en comparación con la de los ancianos y en comparación con la piel fetal tardía.
La vía de señalización mediada por TGF-beta(1) podría estar involucrada en la regulación del desarrollo de la piel en la etapa embrionaria y también en la cicatrización de heridas después del nacimiento. La relativa falta de expresión de los genes TGF-beta(1) y smad2 en pieles de fetos más jóvenes podría contribuir a la curación sin cicatrices.
El proceso normal de cicatrización de heridas
La formación anormal de cicatrices se puede prevenir a través de un proceso eficaz de cicatrización de heridas, pero la inflamación prolongada o persistente en este proceso puede exacerbar la fibrosis cutánea. Por lo tanto, comprender el proceso normal de cicatrización de heridas es crucial para la identificación de la cicatrización aberrante de heridas y la identificación de posibles terapias. En la tabla 1 describimos las etapas del proceso normal de cicatrización de heridas. La figura 1 ilustra el proceso normal de cicatrización de heridas que conduce a la formación de cicatrices.
El proceso de cicatrización de heridas se divide en fases de hemostasia, inflamación, proliferación y remodelación, y para una cicatrización exitosa de heridas, todos los procesos deben ocurrir en la secuencia y el marco de tiempo adecuados. El sangrado debido al trauma conduce a la vasoconstricción local y a la agregación de plaquetas para formar un tapón para llegar a la hemostasia primaria, lo que en consecuencia activa la cascada de coagulación y da como resultado la formación de coágulos de fibrina para formar la hemostasia secundaria. Durante el proceso de hemostasia, las citocinas proinflamatorias y los factores de crecimiento, como el factor de crecimiento derivado de las plaquetas (PDGF), el factor de crecimiento epidérmico (EGF), el factor de crecimiento de fibroblastos 2 (FGF 2; también conocido como bFGF), la interleucina 8(IL-8) y TGF-β, se liberan del coagulo recién formado y de los tejidos dañados circundantes.
La siguiente fase es la fase inflamatoria, en la que las células inflamatorias entran en el área de la herida desde el sistema inmunitario, que se caracteriza por la infiltración secuencial de neutrófilos, macrófagos y linfocitos. La abundancia de neutrófilos no sólo proporciona una defensa crucial contra los microbios invasores, sino que también elimina tanto el patógeno como los desechos de los tejidos en el área de la herida. Esto ocurre a través de la fagocitosis. Los neutrófilos también son esenciales para el reclutamiento de otras células inflamatorias, por ejemplo, macrófagos derivados de monocitos, se diferencian en macrófagos de heridas maduras debido a la influencia de las citoquinas locales, como el interferón-γ (IFN-γ), y los productos bacterianos, como el lipopolisacárido. Los macrófagos maduros continúan el proceso de aclaramiento mediante la fagocitosis de desechos tisulares, organismos microbianos y células apoptóticas, y estos macrófagos con propiedades antimicrobianas se consideran el tipo M1 de macrófago. Después, varios macrófagos M1 sufren apoptosis. Los pocos macrófagos restantes se convierten en el tipo M2 de macrófago como consecuencia de los cambios en la expresión de citoquinas, por ejemplo, IL-13 e IL-4.
Los macrófagos M2 realizan diferentes funciones en el proceso de cicatrización de heridas, ya que son responsables de la transición a la fase proliferativa del proceso de cicatrización de heridas. Los macrófagos M2 liberan factores de crecimiento, como el factor de crecimiento endotelial vascular (VEGF), el PDGF y el TGF-β, que contribuyen al cambio a la fase proliferativa. Estos factores promueven la angiogénesis, la reepitelización y la producción de colágeno. Durante la fase proliferativa, se reclutan fibroblastos y comienzan a producir colágeno, glicosaminoglicanos, proteoglicanos, fibronectina y elastina, que son los principales componentes de la ECM. Los fibroblastos también sufren proliferación, migración y diferenciación debido a la presencia de factores de crecimiento, como FGF, PDGF y TGF-β. Los fibroblastos y las células endoteliales son esenciales para el crecimiento capilar y la formación de tejido de granulación en el sitio de la herida en la dermis reparativa. La contracción de heridas es un proceso crucial en la cicatrización de heridas que se produce a través de la acción de miofibroblastos, que son células contráctiles especializadas, caracterizadas por la expresión de actina muscular lisa α (α-SMA). Estas células desaparecen gradualmente del tejido de granulación a medida que la herida madura. En comparación con los fibroblastos dérmicos normales, los miofibroblastos producen mayores cantidades de componentes de ECM. Curiosamente, las fuentes de miofibroblastos se pueden rastrear en diferentes células, incluidas las células epiteliales de la piel. Sin embargo, la principal fuente de miofibroblastos es la transición o activación de fibroblastos residentes en respuesta a varios desencadenantes, incluido el TGF-β1.
Después de la proliferación y la síntesis de ECM, la cicatrización de heridas avanza a la fase final de remodelación más larga, que es un equilibrio entre la producción, la descomposición y la remodelación de ECM, que continúa durante semanas o meses e incluso, en algunos casos, durante años. Esta fase se caracteriza por la reducción de la proliferación celular, la apoptosis de la mayoría de las células endoteliales, macrófagos y miofibroblastos, la sustitución de los glicosaminoglicanos por proteoglicanos y la sustitución del colágeno III por el colágeno I a través de la acción de las colagenasas. El resultado de la reorganización del ECM es remodelar para formar una arquitectura que se parezca más a los tejidos normales. La manifestación clínica de esta fase es una cicatriz suave palpable, que varía de color rosa a pálido debido a la microvasculatura en la cicatriz. A medida que la vascularización retrocede, el tono de la cicatriz cambia en consecuencia.

Función de la vía dependiente de Smad inducida por TGF-β
La formación de cicatrices es un sistema de reparación eficiente que es importante para la evolución genética de los seres humanos. Sin embargo, cuando una cicatriz recién formada ocupa una gran parte del tejido normal, puede provocar diversos grados de desfiguración y deterioro funcional. No importa el origen de las cicatrices fibrosas, ya sea la formación de cicatrices en la superficie de la piel o la fibrosis de los órganos internos, todas las enfermedades fibróticas están asociadas con la activación de los miofibroblastos productores de ECM, que son los mediadores clave del remodelado del tejido fibrótico. La señalización de TGF-β/Smad en los miofibroblastos se asocia con la formación de cicatrices patológicas, como la formación de cicatrices hipertróficas.
Tab.1

Fig. 2
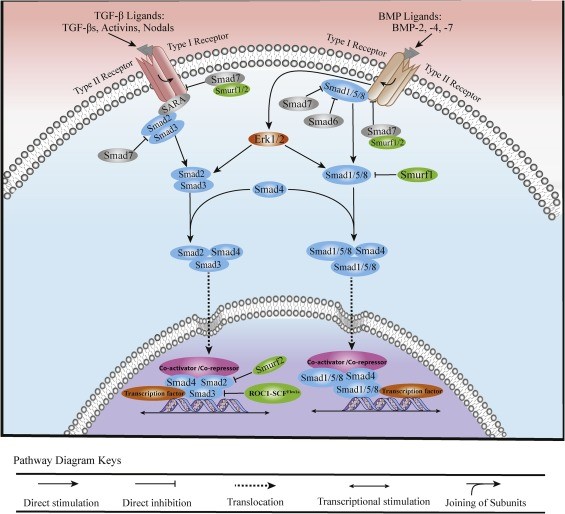
Modulación de la vía dependiente de smad inducida por TGF-β
Dado que la vía dependiente de Smad inducida por TGF-β es crítica para la patogénesis de todas las enfermedades fibróticas, se han investigado varias estrategias terapéuticas para actuar en la vía de señalización y atenuar la formación de cicatrices cutáneas patológicas. Estas estrategias se pueden subdividir en terapéuticas de medicamentos y terapéuticas genéticas y celulares. Los efectos de ambas estrategias terapéuticas se muestran en la Fig.3
Fig. 3

Estrategias terapéuticas de medicamentos
Angiogenina es una molécula potente que induce el crecimiento tumoral al promover la neovascularización, está involucrada en las respuestas inflamatorias y proliferativas durante el proceso de cicatrización de heridas. Además, se ha demostrado que los altos niveles de angiogenina exógena disminuyen la proliferación de fibroblastos y la secreción de TGF-β1.
Baicaleína o 5,6,7-trihidroxiflavona es una terapia prometedora para la antifibrogénesis en la piel ya que ejerce un efecto inhibitorio sobre la vía de señalización TGF-β/Smad2/3 en fibroblastos. Suprime significativamente la proliferación y activación de fibroblastos derivados de la cicatriz hipertrófica e inhibe la expresión de α-SMA.
Ginsenósidos Rg3 (Rg3). Se ha demostrado que Rg3 suprime la proliferación de fibroblastos queloides al disminuir notablemente la expresión del marcador de proliferación Ki-67 de una manera dosis dependiente. Rg3 tiene un efecto inhibitorio sobre las vías de señalización TGF-β/Smad y aumenta los niveles de expresión de ARNm de Smad7.
Kaempferol es una molécula flavonoide, produce antiinflamación e inhibición del crecimiento tumoral. Se ha demostrado que el kaempferol inhibe significativamente la formación de cicatrices hipertróficas a través de la atenuación de la síntesis de colágeno y la supresión de la proliferación y activación de fibroblastos.
Loureirin B es un ingrediente del extracto etanólico de Resina Draconis (RDEE), es eficaz en la profilaxis y el tratamiento de cicatrices aberrantes de la piel. Loureirin B tiene un efecto supresor sobre la expresión de colágeno I, colágeno III y α-SMA en fibroblastos de cicatriz hipertrófica.
Proteína morfogenética ósea-7 (BMP-7) es un miembro de la superfamilia TGF-β. El tratamiento con BMP-7 disminuye notablemente la expresión de α-SMA, TGF-β1 y CTGF y reduce los niveles de colágeno I y III. Además, induce la apoptosis de fibroblastos.
Galangin (3,5,7-trihidroxiflavona) es otro flavonoide activo natural que tiene una actividad antiinflamatoria, puede inhibir significativamente la producción de colágeno e inhibir la proliferación y activación de fibroblastos.
Inhibidores de Enzima convertidora de angiotensina (IECA). Se pueden utilizar para revertir el proceso fibrótico. Estudios recientes han sugerido que tienen un efecto inhibitorio sobre la fibrosis cutánea. Una reducción de la expresión de TGF-β1 y colágeno y una supresión de la proliferación de fibroblastos.
Tab. 2

Posibles estrategias terapéuticas genéticas y celulares
Se han investigado una variedad de técnicas genéticas y celulares para prevenir las cicatrices en la atenuación o el tratamiento de la cicatrización mediante interferencia de ARN (ARNi). El ARNi puede interferir con la transcripción de ciertos genes en fibroblastos y miofibroblastos, lo que podría eliminar la formación de colágeno excesivo, lo que podría reducir las cicatrices aberrantes. Los pequeños ARN interferentes (siARN), ARN de cadena doble simétricos o asimétricos de unos 20 pares de bases, han recibido un interés notable debido a su capacidad para unirse al ARNm.
A pesar de los prometedores resultados con las estrategias terapéuticas celulares y genéticas, la seguridad de estos métodos es cuestionable. Por ejemplo, se ha demostrado que inducen una respuesta inmunitaria a través de la activación del receptor TLR. Por lo tanto, se necesitan más estudios preclínicos y clínicos para evaluar más a fondo la eficacia y la seguridad de estos métodos.
1) Interferencia de ARN por siRNA y shRNA
2) Interferencia de ARN por miRNA
3) Transfección celular
Tab. 3
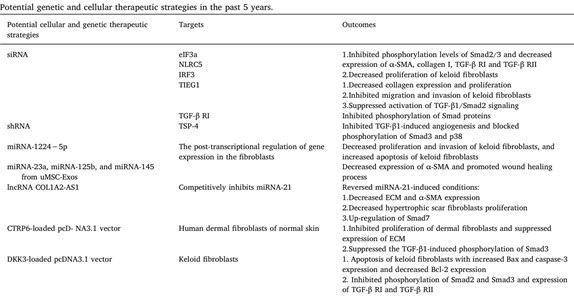
Estrategias terapéuticas combinadas prometedoras
La vía de señalización TGF-β/Smad es la vía canónica involucrada en la formación de colágeno en los fibroblastos y miofibroblastos, y se ha demostrado que múltiples estrategias terapéuticas, incluidas las terapias farmacológicas y los posibles métodos genéticos, inhiben esta vía. Un método de administración eficiente combinado con una terapia dual o incluso una terapia triple que se dirige a la vía de señalización TGF-β/Smad en los fibroblastos o miofibroblastos puede proporcionar un efecto inhibitorio sinérgico significativo en la formación de cicatrices aberrantes en la piel.
Conclusiones
Aunque la formación de cicatrices es un sistema de reparación eficaz para la evolución genética humana, una vez que se produce una cicatriz, no se puede eliminar por completo. Los tejidos de la cicatriz ocupan las estructuras de los tejidos normales originales, lo que afecta gravemente a sus funciones y estética normales. Las terapias que pueden restaurar la función y la apariencia del tejido dañado son de gran interés. En la actualidad, la profilaxis y el tratamiento de las cicatrices son una preocupación mundial. En general, las opciones de tratamiento para las cicatrices se pueden dividir en tres clases, ya sea tratamiento quirúrgico, tratamiento no quirúrgico o la combinación de ambas. La formación de cicatrices fibróticas aberrantes es el resultado final del proceso de cicatrización de heridas patológicamente desorganizado. Por lo tanto, interferir con este proceso puede reducir la fibrosis hasta cierto punto, evitando así la fibrosis excesiva.
Se ha logrado un gran progreso en la comprensión de los mecanismos básicos de cómo los fibroblastos y los miofibroblastos leen la señalización TGF-β/Smad en condiciones patológicas y producen un gran número de colágenos desordenados que conducen a la formación de cicatrices aberrantes. Sin embargo, actualmente no hay medicamentos disponibles para la inhibición completa de la fibrosis, y todavía hay limitaciones en el tratamiento estándar de las cicatrices aberrantes. Como se ha demostrado que las monoterapias múltiples ejercen efectos inhibitorios en la vía canónica de señalización TGF-β/Smad y se ha informado de que las terapias combinadas prometedoras inhiben significativamente la fibrosis en otros órganos, planteamos la hipótesis de que la combinación de algunos de los tratamientos de monoterapia mencionados anteriormente puede tener un notable efecto inhibidor sinérgico. Sin embargo, no importa cómo intervenga artificialmente en el proceso de formación de cicatrices, el grado de fibrosis solo se puede atenuar posiblemente en la mayor medida posible, y actualmente no se puede lograr la curación sin cicatrices. Los estudios han demostrado que la piel fetal lesionada puede regenerarse al principio del embarazo sin la formación de tejido cicatricial, lo que sugiere que la curación sin cicatrices es posible. La curación sin cicatrices implica la regeneración celular, en lugar de la reparación. Los numerosos factores de crecimiento y células madre presentes en el líquido amniótico humano proporcionan una condición indispensable para la regulación precisa de la regeneración celular. Aunque se requieren más estudios para comprender mejor este proceso, se puede lograr una curación sin cicatrices proporcionando un microambiente similar al del líquido amniótico.


